はじめに:生命の設計図を書き換える「魔法のハサミ」
もし、あなたが「生命の設計図」を自由に書き換える力を手に入れたとしたら、何をしますか?
生まれつき抱える病気の原因となる遺伝子を修正するでしょうか。あるいは、人類を長年苦しめてきた、がんやウイルス感染症を根絶するでしょうか。それとも、異常気象にも負けず、栄養価の高い作物を生み出し、世界から飢餓をなくすことに使うでしょうか。
かつては神の領域とされ、SF小説の題材でしかなかった「生命のプログラムの書き換え」。それが今、**「CRISPR-Cas9(クリスパー・キャスナイン)」**という一つのテクノロジーによって、現実のものとなりつつあります。
この言葉に、何やら難解なイメージを抱くかもしれません。しかし、その本質は驚くほどシンプルで、かつパワフルです。CRISPR-Cas9は、しばしば**「遺伝子のハサミ」**と表現されます。広大な遺伝情報の中から、目的の場所だけを正確に見つけ出し、狙った通りに「切断」し、「編集」することを可能にする、まさに魔法のようなツールなのです。
この技術の登場は、生物学の世界に地殻変動ともいえるほどの衝撃を与えました。2020年には、その開発者であるエマニュエル・シャルパンティエ博士とジェニファー・ダウドナ博士がノーベル化学賞を受賞したことからも、その重要性がうかがえます。
この記事では、まさに今、私たちの未来を根底から変えようとしているCRISPR-Cas9のすべてを、可能な限り分かりやすく、そして深く掘り下げていきます。
- 第1章では、CRISPR-Cas9が「そもそも何なのか?」という基本の仕組みを、身近なものに例えながら解き明かします。
- 第2章では、遺伝病やがん治療といった医療分野で、実際に人々の命を救い、人生を変えた感動的な実例を紹介します。
- 第3章では、私たちの食卓にも関わる、農業や食料生産における驚くべき応用例を見ていきます。
- 第4章では、さらに進化した次世代のゲノム編集技術にも触れ、テクノロジーの未来を展望します。
- そして第5章では、この強力すぎる技術がもたらす「光」だけでなく、「影」の部分、つまり私たちが真剣に向き合わなければならない倫理的な課題について考えていきます。
これは、単なる科学技術の解説記事ではありません。生命とは何か、人間とは何か、そして私たちはどのような未来を選択すべきか、という根源的な問いを、あなた自身に投げかける物語でもあります。さあ、生命科学の最前線を巡る、知的好奇心に満ちた旅に出かけましょう。
第1章:CRISPR-Cas9って一体何?初心者にもわかる基本の「き」
CRISPR-Cas9という名前は、何かの呪文のように聞こえるかもしれません。しかし、その発見のきっかけは、私たちの食生活に意外なほど身近な存在、**「ヨーグルト」**の研究にありました。
細菌が持つ「記憶」と「反撃」のシステム
話は1980年代に遡ります。日本の研究者が大腸菌のゲノム(全遺伝情報)の中に、奇妙な繰り返し配列を発見しました。これが後に「CRISPR」と呼ばれる部分です。当初、その機能は全くの謎でした。
転機が訪れたのは2000年代。ヨーグルトやチーズの製造に欠かせない乳酸菌を研究していた科学者たちが、面白い事実に気づきます。ウイルスに感染しても生き延びた乳酸菌は、その子孫も同じウイルスに強くなるのです。まるで、人間が一度かかった病気に対する免疫を持つように。
調査を進めると、ウイルスの攻撃を生き延びた菌のCRISPR配列の中に、なんと攻撃してきたウイルスのDNAの一部が組み込まれていることが判明しました。これは驚くべき発見でした。細菌は、敵の情報を自らの遺伝情報に「記録」し、一種の「記憶」として保持していたのです。
そして、再び同じウイルスが侵入してくると、細菌はこの「記憶」を元に行動を開始します。
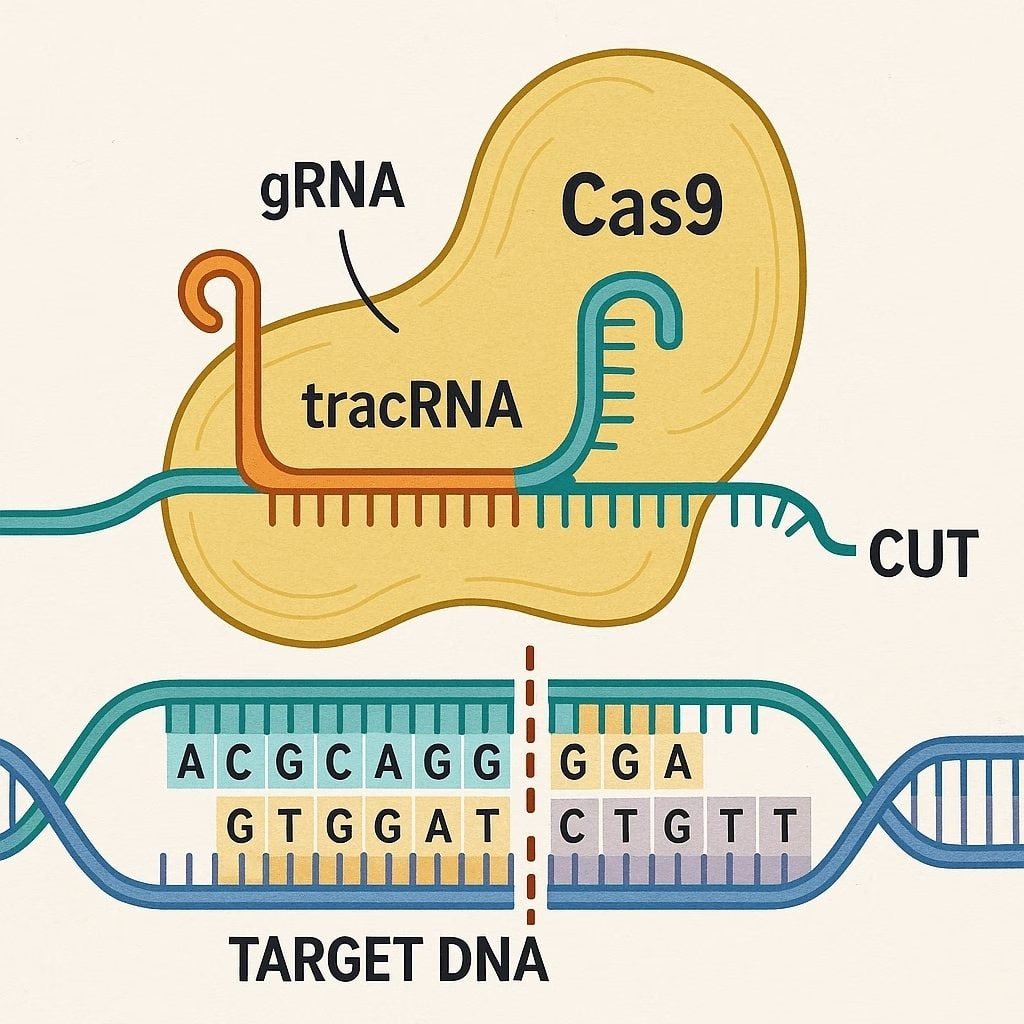
- まず、記録しておいたウイルスのDNA情報をコピーして**「ガイドRNA(gRNA)」**という分子を作ります。これは、侵入者(ウイルス)の顔写真が貼り付けられた「指名手配書」のようなものです。
- 次に、この指名手配書(ガイドRNA)を、**「Cas9(キャスナイン)」**というタンパク質に渡します。Cas9は、DNAを切断する能力を持つ「ハサミ」の役割を果たします。
- 指名手配書を持ったハサミ(ガイドRNAとCas9の複合体)は、細胞内をパトロールします。
- そして、指名手配書の顔写真とピッタリ一致するDNA配列(侵入してきたウイルスのDNA)を見つけると、即座にその場所を**「カシャッ!」**と切断してしまうのです。
DNAを切断されたウイルスは、もはや増殖することができず、無力化されます。これが、細菌が太古の昔から進化の過程で獲得してきた、驚くほど巧妙なウイルス撃退システム、すなわち**「獲得免疫システム」**の正体でした。
「細菌の免疫」を「万能の編集ツール」へ
この発見に、科学者たちは震えました。「もし、この仕組みを細菌以外の細胞、例えば人間の細胞でも動かすことができたら?」「そして、指名手配書であるガイドRNAの配列を、ウイルスのDNAではなく、私たちが狙いたい任意の遺伝子の配列に置き換えたら?」
そのアイデアを実現したのが、前述のシャルパンティエ博士とダウドナ博士でした。彼女たちは、この細菌の免疫システムを、人間を含むあらゆる生物の細胞で機能する、**汎用的な「ゲノム編集ツール」**として再設計することに成功したのです。
CRISPR-Cas9の仕組みを、私たちの世界に例えるなら、こうなります。
- Cas9タンパク質: 非常に高性能な「ハサミ」。
- ガイドRNA: 編集したい場所の「住所(DNA配列)」が書かれたメモ。
- 細胞: 広大な図書館。
- ゲノム(DNA): 図書館に収められた、膨大な蔵書。
あなたが、ある蔵書(ゲノム)の中の、特定のページ(遺伝子)にある、たった一つの誤字(遺伝子の変異)を修正したいとします。
従来の技術では、目的のページを探し出すだけで膨大な時間と労力が必要でした。図書館全体を虱潰しに探すようなものです。
しかし、CRISPR-Cas9を使えば、「〇〇という本の△△ページの□行目」という住所が書かれたメモ(ガイドRNA)をハサミ(Cas9)に渡すだけで、ハサミは自動的にその場所を探し出し、誤字の部分を正確に切断してくれるのです。
切断されたその後は?生命が持つ「修復力」を利用する
では、DNAが切断された後はどうなるのでしょうか?ここでも、生命が元々持っている素晴らしい能力が利用されます。細胞には、傷ついたDNAを自分で修復する仕組みが備わっているのです。修復の仕方には、主に2つのパターンがあります。
- 非相同末端結合(NHEJ):これは、いわば「応急処置」のような修復方法です。切れたDNAの断片を、とにかく急いでつなぎ合わせようとします。しかし、この過程で数文字の欠落や挿入といった「修復ミス」が起こりやすく、結果的にその場所の遺伝子の機能が失われる(ノックアウトされる)ことが多くなります。特定の遺伝子の働きを止めたい場合に利用されます。
- 相同組換え修復(HDR):こちらは、より精密な「設計図通りの修復」です。細胞は、切断された部分の「お手本」となる正常なDNA配列(鋳型DNA)があると、それを見本にして正確に修復しようとします。科学者たちは、この仕組みを利用し、**正常な遺伝子配列を書き込んだ「お手本(鋳型DNA)」を、CRISPR-Cas9と一緒に細胞に入れてやります。**すると、切断された部分が、そのお手本通りに書き換えられるのです。これにより、異常な遺伝子を正常な遺伝子に「修正」したり、新たな遺伝子を「挿入」したりすることが可能になります。
このように、CRISPR-Cas9は「切る」だけでなく、生命が本来持つ「治す」力を巧みに利用することで、遺伝情報を自在に「編集」することを実現した画期的な技術なのです。その操作の簡便さ、正確さ、そしてコストの低さは、それまでのゲノム編集技術とは比較にならず、世界中の研究室に瞬く間に普及しました。そして、その応用は、医療や農業の分野で、目覚ましい成果を生み出し始めています。
第2章:医療に革命を!遺伝病との闘いに差し込む光
人類の歴史は、病との闘いの歴史でもありました。特に、生まれつき遺伝子に異常があることで発症する遺伝性疾患は、根本的な治療法がなく、多くの患者さんとその家族を苦しめてきました。しかし、CRISPR-Cas9の登場により、その長く暗いトンネルに、ついに光が差し込み始めています。
ケース1:鎌状赤血球症 – 「人生が変わった」ヴィクトリア・グレイさんの物語
ヴィクトリア・グレイさんは、米国ミシシッピ州に住む女性です。彼女は生まれつき**「鎌状赤血球症」**という重い遺伝性の血液疾患を抱えていました。
この病気は、赤血球の形を決めるヘモグロビン遺伝子のたった1つの塩基が間違っているために発症します。正常な赤血球がドーナツのような形をしているのに対し、鎌状赤血球症の患者の赤血球は、硬い「鎌(かま)」のような形に歪んでしまいます。
この歪んだ赤血球は、血管の中で詰まりやすく、激しい痛み(クリーゼと呼ばれる発作)、臓器障害、脳梗塞、感染症など、命に関わる深刻な症状を引き起こします。ヴィクトリアさんも、幼い頃から入退院を繰り返し、激痛に耐える日々を送っていました。輸血が欠かせず、夢だった仕事も諦めざるを得ませんでした。
彼女の運命を劇的に変えたのが、CRISPR-Cas9を用いた臨床試験でした。
2019年、ヴィクトリアさんは、この革新的な治療を受ける最初の患者の一人となったのです。治療のプロセスはこうです。
- まず、ヴィクトリアさんの体内から血液の元となる細胞**「造血幹細胞」**を取り出します。
- 体外に取り出したこの細胞に、CRISPR-Cas9を使って遺伝子編集を行います。ここで狙うのは、病気の原因であるヘモグロビン遺伝子そのものではありません。科学者たちは、もっと賢い方法を考え出しました。人間は、胎児のときには「胎児ヘモグロビン」という別の種類のヘモグロビンを作っています。これは酸素を運ぶ能力が非常に高く、鎌状になりません。通常、胎児ヘモグロビンの生産は生後まもなく停止するのですが、その生産を抑制している**「BCL11A」**という遺伝子があります。
- そこで、CRISPR-Cas9を使い、この**BCL11A遺伝子の働きを「オフ」**にするのです。
- 遺伝子編集によって、再び胎児ヘモグロビンを作れるようになった造血幹細胞を、大量に培養します。
- 最後に、これらの細胞をヴィクトリアさんの体内に戻します。
結果は、驚くべきものでした。体内に戻された造血幹細胞は、正常な機能を持つ胎児ヘモグロビンを豊富に含んだ赤血球を作り始めました。治療から数ヶ月後、彼女を長年苦しめてきた激しい痛みの発作は消え、輸血も必要なくなりました。
「CRISPRは私の人生を変えました」と彼女は語ります。「病気に支配されるのではなく、自分で人生をコントロールできるようになったのです」。
この治療法は**「Casgevy」**という名前で、2023年に英国と米国で、鎌状赤血球症および、同様にヘモグロビンの異常で起こる「βサラセミア」という遺伝病の治療薬として、世界で初めて承認されました。これは、CRISPR技術が基礎研究の段階を越え、現実の医療として人々の元に届いた歴史的な瞬間でした。
ケース2:がん治療 – 免疫細胞を「最強の兵士」に改造する
がん治療の世界でも、CRISPR-Cas9は大きな期待を集めています。特に注目されているのが、**「CAR-T(カーティー)細胞療法」**との組み合わせです。
CAR-T細胞療法とは、患者自身の免疫細胞(T細胞)を取り出し、がん細胞を特異的に見つけて攻撃できるように遺伝子改変を加えて体内に戻す、という画期的な治療法です。いわば、体内の免疫細胞を「がん攻撃専門の特殊部隊」に訓練し直すようなものです。
この治療法は、一部の血液がんで劇的な効果を上げていますが、いくつかの課題も抱えています。例えば、がん細胞が免疫細胞からの攻撃を逃れるために「ブレーキ」をかける仕組み(免疫チェックポイント)を持っていることや、固形がん(臓器などにできる塊状のがん)には効きにくいことなどです。
そこで、CRISPR-Cas9の出番です。研究者たちは、CAR-T細胞を作る際に、CRISPR-Cas9を使って**さらなる「チューンナップ」**を施そうとしています。
- ブレーキの破壊: T細胞が持つ免疫のブレーキ役となる遺伝子(例えばPD-1)を、CRISPR-Cas9で予めノックアウト(破壊)しておく。これにより、がん細胞がブレーキをかけてきても、T細胞はひるむことなく攻撃を続けることができます。
- ステルス機能の付与: 正常な免疫システムから異物とみなされないよう、T細胞自身の目印となる遺伝子を消し、より長く体内で戦えるようにする。
- 汎用性の獲得: 現在のCAR-T療法は、患者一人ひとりから細胞を取り出して作る「オーダーメイド治療」であり、非常に高額で時間もかかります。そこで、健康なドナー(提供者)から作ったT細胞を、CRISPR-Cas9で編集して、誰にでも使える「既製品(オフ・ザ・シェルフ)」のCAR-T細胞を作る研究が進められています。
すでに、こうした次世代のCRISPR-CAR-T療法の臨床試験が世界中で始まっており、従来の治療法では効果がなかった難治性のがん患者で、有望な結果が報告され始めています。これは、がんとの闘いにおける、新たな強力な武器となる可能性を秘めています。
ケース3:失明からの回復 – 眼という特別な舞台での挑戦
遺伝性の病気の中には、視力を奪うものも少なくありません。**「レーバー先天性黒内障(LCA)」**は、乳幼児期に発症し、重度の視力障害や失明に至る遺伝性網膜疾患です。原因となる遺伝子は複数知られていますが、その一つに「CEP290」遺伝子の変異があります。
眼は、CRISPR-Cas9を用いた治療にとって、いくつかの好都合な点があります。
- 眼球は比較的小さく、閉鎖的な空間であるため、治療薬を直接注入しやすく、全身に広がるリスクが低い。
- 免疫反応が起きにくい場所(免疫特権部位)とされている。
- 片方の眼で効果と安全性を試し、もう片方の眼と比較することができる。
2020年、世界で初めて、CRISPR-Cas9治療薬を患者の体内に直接投与する臨床試験が、このLCAを対象に始まりました。これは、ヴィクトリアさんのように一度細胞を体外に取り出すのではなく、注射によってCRISPR-Cas9を網膜の細胞に直接送り込み、その場で遺伝子を編集するという、より高度な挑戦です。
2023年に発表された中間報告では、治療を受けた患者の一部で、光を感知する能力の改善や、暗い場所での視力の向上といった効果が確認されました。まだ研究は道半ばですが、これまで治療法がなかった遺伝性眼疾患の患者にとって、一筋の光明が差し込んだことは間違いありません。
これらのケースは、CRISPR-Cas9がもたらす医療革命の、ほんの序章に過ぎません。デュシェンヌ型筋ジストロフィー、ハンチントン病、嚢胞性線維症など、数多くの遺伝性疾患に対する治療法の開発が、驚異的なスピードで進んでいます。
第3章:食卓から地球を救う?農業と食料生産の未来
CRISPR-Cas9の革命は、医療の分野だけにとどまりません。私たちが毎日口にする「食」の世界、すなわち農業や水産業においても、その技術は静かに、しかし確実に未来を変えようとしています。人口増加、気候変動、環境問題といった地球規模の課題に、ゲノム編集技術がどのように貢献できるのでしょうか。
従来の品種改良との違い
まず理解しておきたいのは、ゲノム編集と**「遺伝子組換え(GMO)」**との違いです。
- 遺伝子組換え(GMO): 他の生物(例えば、細菌や別の植物)から持ってきた「外来の遺伝子」を、作物のゲノムに組み込む技術です。
- ゲノム編集(CRISPR-Cas9など): 作物が元々持っている遺伝子を狙って、その一部の働きを強めたり、弱めたり、あるいはオフにしたりする技術です。外から新しい遺伝子を持ち込むのではなく、あくまで「内在する遺伝子の編集」である点が大きな違いです。
ゲノム編集による作物の改良は、自然界で起こる「突然変異」や、これまで何千年もの歳月をかけて行われてきた「品種改良」のプロセスを、超高速かつ高精度に行うもの、と捉えることができます。
ケース4:高GABAトマト – 日本発、身近になったゲノム編集食品
日本において、ゲノム編集技術を応用した食品として初めて市場に登場し、大きな話題を呼んだのが**「高GABAトマト」**です。
GABA(ギャバ、γ-アミノ酪酸)は、血圧を下げる効果や、リラックス効果をもたらすことで知られるアミノ酸の一種です。トマトは元々GABAを含んでいますが、その量はそれほど多くありません。
筑波大学の研究チームは、CRISPR-Cas9を用いて、トマトが持つ「GABAを分解してしまう酵素」を作る遺伝子を狙って、その働きをオフにしました。すると、作られたGABAが分解されずにトマトの中に蓄積され、通常のトマトの4〜5倍ものGABAを含むトマトが誕生したのです。
重要なのは、このトマトには外来の遺伝子は一切導入されていないという点です。元々持っている遺伝子の機能を少し変えただけなので、安全性は従来のトマトと変わらないとされています。日本では、こうしたゲノム編集食品は、届け出をすれば販売が可能となっており、2021年から苗の家庭菜園向けの提供や、ピューレなどの加工品の販売が始まっています。
これは、ゲノム編集技術が、特定の病気を持つ人だけでなく、私たちの健康増進や生活の質の向上に直接貢献できる可能性を示した、象徴的な事例と言えるでしょう。
ケース5:病気に強い作物 – 持続可能な農業への道
世界の農業が直面する大きな課題の一つが、病害による収穫量の減少です。これを防ぐために大量の農薬が使われていますが、それは環境への負荷や、生産コストの増大につながります。
ゲノム編集は、この問題に対する強力な解決策となる可能性があります。
- うどんこ病に強い小麦: 小麦を悩ませる主要な病気である「うどんこ病」。研究者たちは、この病気の原因菌が感染する際に利用する、小麦の「Mlo」という遺伝子を発見しました。そして、CRISPR-Cas9でこのMlo遺伝子を破壊したところ、うどんこ病菌が感染できない、高い耐性を持つ小麦を作り出すことに成功しました。
- いもち病に強いイネ: アジアの稲作に壊滅的な被害をもたらす「いもち病」に対しても、同様のアプローチで耐性を持つイネの開発が進んでいます。
- 干ばつや塩害に強い作物: 気候変動により、世界中で干ばつや土壌の塩類化が深刻化しています。作物が持つ乾燥や塩分へのストレス応答に関わる遺伝子をゲノム編集で調節し、厳しい環境でも育つタフな作物を生み出す研究も、世界中で活発に行われています。
これらの技術が実用化されれば、農薬の使用量を大幅に削減し、これまで農業に適さなかった土地でも食料生産が可能になるかもしれません。それは、環境に優しく、持続可能な農業の実現に向けた大きな一歩となります。
ケース6:肉厚なマダイ – 水産業にも広がるイノベーション
ゲノム編集の波は、水産業にも及んでいます。京都大学と近畿大学の研究グループは、CRISPR-Cas9を用いて、より効率的に成長するマダイやトラフグを開発しました。
彼らが狙ったのは、**「ミオスタチン」**という遺伝子です。この遺伝子は、筋肉が付きすぎるのを抑える「ブレーキ」の役割を果たしています。このミオスタチン遺伝子をCRISPR-Cas9で破壊したところ、通常のマダイに比べて筋肉量が平均で約1.2倍に増加した「肉厚マダイ」が誕生したのです。トラフグでも同様に、成長が早く可食部が多い個体が生み出されています。
より少ないエサで、より早く、より多くの可食部が得られる魚を養殖できれば、食料増産に大きく貢献できます。この「肉厚マダイ」も、高GABAトマトと同様に届け出が行われ、一部で試験販売が開始されています。
その他にも、アレルギーの原因となる物質(アレルゲン)を含まないソバや卵、カフェインの量を減らしたコーヒー豆など、ゲノム編集技術が拓く「食」の可能性は、とどまるところを知りません。それは、私たちの食卓をより豊かに、そして安全にするだけでなく、地球規模の食料・環境問題に対する、希望の光となり得るのです。
第4章:進化するテクノロジー – CRISPR-Cas9のその先へ
CRISPR-Cas9は、間違いなく革命的なツールです。しかし、どんな強力なツールにも、限界や課題は存在します。科学者たちは、その「神の技術」に満足することなく、さらなる高みを目指して、技術の改良と進化を続けています。
CRISPR-Cas9が抱える課題:「オフターゲット」問題
CRISPR-Cas9の最大の課題の一つが、**「オフターゲット効果」**です。
これは、ガイドRNAが狙った目的のDNA配列(オンターゲット)だけでなく、よく似た別の配列を間違って切断してしまう現象を指します。いわば「誤爆」です。
図書館の例で言えば、目的のページと非常によく似た記述が別の本にもあり、ハサミがそちらも間違って切ってしまうようなものです。もし、この誤爆が、がんの発生を抑える重要な遺伝子や、生命維持に不可欠な遺伝子の上で起きてしまったら、予期せぬ深刻な副作用を引き起こす可能性があります。
このオフターゲットのリスクをいかに低減するかは、CRISPR-Cas9を安全な医療技術として確立する上で、最も重要な課題です。科学者たちは、Cas9タンパク質そのものを改良して精度を高めたり、ガイドRNAの設計を工夫したり、治療薬を目的の細胞だけに届ける「デリバリー技術」を向上させたりと、多角的なアプローチでこの問題に取り組んでいます。
そして、この課題を根本的に解決する可能性を秘めた、新しい世代のゲノム編集技術も登場しています。
「ハサミ」から「鉛筆と消しゴム」へ:ベース編集とプライム編集
CRISPR-Cas9がDNAの二本鎖を「バッサリ」と切断する「ハサミ」だとすれば、これから紹介する新技術は、より繊細な操作を可能にする**「鉛筆と消しゴム」**に例えられます。
1. ベース編集(塩基編集)
遺伝情報は、A(アデニン)、T(チミン)、G(グアニン)、C(シトシン)という4種類の塩基の並び方で決まります。遺伝病の多くは、このたった1つの塩基が別のものに置き換わってしまう「点突然変異」によって引き起こされます。
ベース編集(Base Editing)は、DNAを切断することなく、この1塩基だけをピンポイントで書き換える技術です。
- まず、切断能力を失わせたCas9(デッドCas9)に、「脱アミノ酵素」という特殊な酵素を融合させます。
- このツールがガイドRNAに導かれて目的の場所に行くと、脱アミノ酵素が働き、例えば「C」の塩基を「T」に、あるいは「A」の塩基を「G」に、直接変換するのです。
DNAを切断しないため、NHEJのような予期せぬ修復ミスや、大規模な欠失・挿入が起こるリスクを大幅に減らすことができます。鎌状赤血球症の原因となる点突然変異などを、より安全に、かつ効率的に修正できると期待されています。まるで、文章中の誤字を消しゴムで消し、正しい文字を鉛筆で書き込むような、エレガントな編集技術です。
2. プライム編集
ベース編集は非常に強力ですが、書き換えられる塩基のパターン(C→T、A→G)には制限がありました。そこで、さらに自由度の高い編集を目指して開発されたのが**「プライム編集(Prime Editing)」**です。
プライム編集は、「探して、置き換える(search-and-replace)」と表現される、さらに洗練された技術です。
- このツールでは、切断能力を弱めたCas9に、「逆転写酵素」という別の酵素が取り付けられています。
- そして、ガイドRNA(プライム編集ガイドRNA、pegRNAと呼ばれる)には、標的配列の情報に加えて、「書き換えたい正しい塩基配列」の情報も予め組み込まれています。
- ツールが標的部位に結合すると、まずDNAの一方の鎖だけをそっと切断(ニックを入れる)。その後、逆転写酵素がpegRNAに書かれたお手本を元にして、切断した部分を望みの配列に直接書き換えてしまうのです。
プライム編集は、1塩基の置換だけでなく、数塩基の短い配列を挿入したり、削除したりすることも可能です。理論的には、点突然変異によって引き起こされる遺伝病の約90%を修正できる可能性があるとされ、究極のゲノム編集技術の一つとして、世界中の研究者がその改良と応用にしのぎを削っています。
これらの次世代技術は、まだ研究開発の初期段階にありますが、ゲノム編集をより安全で、より精密なものへと進化させ、これまで治療が困難だった多くの疾患に新たな希望をもたらすものと、大きな期待が寄せられています。テクノロジーは、常にその限界を自ら打ち破りながら、前進を続けているのです。
第5章:光と影 – 私たちが向き合うべき倫理的な課題
CRISPR-Cas9とその進化形がもたらす恩恵は、計り知れません。遺伝病に苦しむ人々を救い、難治性のがんに立ち向かい、食料危機を解決する。その輝かしい「光」の部分に、私たちは大きな希望を抱きます。
しかし、これほどまでに強力で、生命の根幹に介入する技術は、同時に深く、重い問いを私たちに投げかけます。それは、技術の「影」の部分、すなわち倫理的・社会的な課題です。この問題から目を背けて、未来を語ることはできません。
禁断の扉:「デザイナーベビー」と生殖細胞系列の編集
CRISPR-Cas9に関する倫理的議論の中で、最も大きな懸念を呼んでいるのが**「生殖細胞系列のゲノム編集」**です。
これまでの章で紹介してきた治療法は、すべて**「体細胞のゲノム編集」です。体細胞(血液、筋肉、神経などの細胞)への編集は、その患者さん個人の病気を治すためのものであり、その遺伝的な変更が子孫に受け継がれることはありません。**
一方、「生殖細胞系列のゲノム編集」は、精子、卵子、あるいは受精卵といった、次世代へと遺伝情報を伝える細胞に対して行われます。ここになされた変更は、その子供だけでなく、孫、ひ孫へと、未来永劫にわたって人類の遺伝子プールの中に受け継がれていくことになります。
病気の遺伝子を根本から断ち切り、子孫に遺伝させないようにできる、という側面は魅力的かもしれません。しかし、その扉を開けることは、多くの深刻な問題を引き起こします。
- 安全性の問題: もし、受精卵の段階でオフターゲット効果(誤爆)や予期せぬ遺伝子変異が起きたらどうなるでしょうか。それは、生まれてくる子供の全身に影響を及ぼし、全く新しい、予測不能な疾患を生み出すかもしれません。しかもその影響は、永続的に子孫に伝わります。
- 「治療」と「強化」の境界線: どこまでが許容される「治療」で、どこからが許されない「強化(エンハンスメント)」なのでしょうか。病気の治療は良いとしても、例えば、身長を高くする、筋肉を付きやすくする、知能を高める、といった目的で遺伝子を編集することは許されるのでしょうか。
- デザイナーベビーの誕生: こうした「強化」が野放しになれば、親が望む外見や能力を持つように遺伝子を操作された**「デザイナーベビー」**が生まれる可能性があります。それは、経済的に裕福な層だけが優れた遺伝子を手に入れ、社会に新たな格差と差別を生み出す、ディストピア的な未来につながりかねません。
2018年、世界中の科学者を震撼させる事件が起こりました。中国の研究者、賀建奎(が・けんけい)氏が、CRISPR-Cas9を使ってHIV(エイズウイルス)に感染しないように遺伝子を編集した双子の女児を誕生させたと発表したのです。この行為は、科学的にも倫理的にも極めて問題が多く、世界の科学界から厳しい非難を浴びました。この事件は、私たちがまさに「禁断の扉」の前に立っているという事実を、全世界に突きつけました。
現在、多くの国では、法律やガイドラインによって生殖細胞系列のゲノム編集を臨床応用することは固く禁じられています。技術的に可能であることと、社会的に許容されるべきことは、全く別の問題なのです。
その他の倫理的・社会的課題
生殖細胞系列の問題以外にも、考えるべき課題は山積しています。
- 治療へのアクセスの格差: Casgevyのような画期的な治療法が承認されましたが、その薬価は一人あたり数億円と、極めて高額です。これでは、恩恵を受けられるのはごく一部の富裕層に限られてしまいます。「命の値段」に格差があって良いのでしょうか。誰もが必要な治療を受けられる社会制度をどう構築していくか、という重い課題が残されています。
- 長期的な影響の不確実性: CRISPR-Cas9による治療の歴史はまだ浅く、数十年単位での長期的な安全性や影響については、まだ誰にも分かりません。慎重な追跡調査と、透明性の高い情報公開が不可欠です。
- 生態系への影響: ゲノム編集された作物や家畜が、自然界の生態系にどのような影響を与えるのか、という懸念もあります。例えば、特定の害虫に極端に強い作物が普及することで、その害虫を食べる他の生物の食料がなくなったり、逆にその耐性を打ち破る、さらに強力な「スーパー害虫」の出現を促したりする可能性もゼロではありません。
これらの課題に、簡単な答えはありません。科学者だけが考えるのではなく、法律家、倫理学者、宗教家、そして私たち市民一人ひとりが、この技術が持つ意味を理解し、その使い方についてオープンに、そして真剣に議論していく必要があります。
おわりに:未来の扉を開けるのは、私たち自身の選択
CRISPR-Cas9という「生命のハサミ」を手に入れた人類は、今、大きな岐路に立っています。
目の前には、遺伝病やがん、食糧問題といった、人類が長年抱えてきた苦しみを克服できるかもしれない、希望に満ちた未来への扉があります。ヴィクトリア・グレイさんのように、病気の軛(くびき)から解放され、新たな人生を歩み始める人々が、これからますます増えていくでしょう。私たちの食卓はより豊かになり、地球環境との共存も可能になるかもしれません。
しかしその隣には、生命を商品のように扱い、格差と差別を助長する、ディストピア的な未来へと続く扉も存在します。一度開けてしまえば、二度と元には戻れない、パンドラの箱です。
どちらの扉を開けるのか。その鍵を握っているのは、一部の科学者や政治家だけではありません。この技術の恩恵を受け、同時にそのリスクを負うことになる、私たち一人ひとりです。
CRISPR-Cas9は、もはや遠い世界の科学の話ではありません。それは、私たちの健康、食、そして「人間とは何か」という価値観そのものに深く関わる、**「自分ごと」**なのです。
だからこそ、私たちはこの技術について学び、知る必要があります。その仕組みを理解し、可能性とリスクの両方を正しく天秤にかける。そして、社会全体で対話し、賢明なルールを作っていく。技術の暴走を防ぎ、その恩恵を最大化するためには、科学の進歩と、社会の成熟が、両輪となって進んでいくことが不可欠です。
生命の設計図を書き換えるという、かつて神にしか許されなかった力。その力を、人類は果たして賢く、そして倫理的に使いこなすことができるのでしょうか。
その答えは、まだ誰にも分かりません。未来は、この記事を読んでいるあなた自身の、そして私たちの選択にかかっています。この驚異のテクノロジーが、絶望を希望に変え、すべての人々にとって明るい未来を照らす光となることを、心から願ってやみません。


 ブロトピ:今日のブログ更新
ブロトピ:今日のブログ更新
コメント